流式细胞术已广泛应用于临床检验,但其质量控制面临三大难题:实验室标准不统一、操作数据分析易受人为误差影响、无室间质评项目准确性难保障。
中华检验医学杂志2025年3月第48卷第3期《流式细胞术临床检验质量控制专家共识》,从人员管理、标本处理、试剂耗材、仪器校准、室内质控、室间评价六大环节建立标准化流程,旨在提升检测准确性,推动行业规范化发展。
共识11核心要点
● 必须做性能验证
新项目启用、更换设备/试剂、仪器维修后,需验证正确度、精密度、线性范围。
● 明确参考区间
淋巴细胞亚群等数值类检测需设定实验室自己的参考区间,区分成人/儿童,验证至少用20名健康人(性别年龄均衡),异常值需重新验证。
● 规范报告流程
完整记录患者信息及参考区间,补充异常细胞群分析,及时与临床沟通。
● 数据安全存档
原始数据至少保存2年,禁止连接外部设备,确保数据真实可追溯。
● 强推荐执行!
室内与室间质量控制
(一)室内质量控制
开展流式细胞临床检测的实验室应制订室内质量控制程序,室内质量控制应包括从实验室接收标本到发布报告的全过程。
1.每日质控检测
(1)质控微球检测:每日开机初始化后,需使用厂家推荐的质控荧光微球和质控软件对仪器激光功率、荧光通道 CV 及电压变化值等进行检测,检测结果应符合厂家推荐使用要求。
(2)细胞质控物检测:应选择商品化的细胞质控物。一般实验室可以选择类型为高值的细胞质控物,艾滋病检测实验室应同步选择低值和高值2种类型的细胞质控物。每日检测样品之前,应检测细胞质控物。根据质控结果绘制L-J质控图,同时采用 Westgard 质控规则(建议至少使用13S、22S规则)进行质控结果分析。确认质控在控后,才能进行当日的标本检测。
2. 结果报告时的质控
结果报告时,需分析结果的可靠性。如:T、B和NK细胞相对计数的总和应占淋巴细胞总数的100%±5% 范围内;CD4+T细胞和CD8+T细胞百分比的总和正常情况下应等同于 CD3+T细胞的百分比,变化范围在 5%~10%内。标本中该细胞群阳性率大于30%前提下,多管CV值应不大于8%,标本中该细胞群阳性率小于30%时,多管CV值应不大于15%。
3. 失控后的管理与改进
出现失控情况时,必须立即查找、分析导致失控的原因,采取纠正措施,评估失控对检验结果的影响,并及时填写失控记录表。如果失控类型为随机误差,则需复查质控物,复查结果在控后,即可进行标本检测;如果复查结果仍然失控或失控类型为系统误差,则需对仪器、试剂等检测体系进行排查,查找原因并纠正,同时对以往标本检测结果的准确性进行评估,如有必要需召回报告并重新检测。必要时还需启动针对性的预防措施,防止同类问题再次发生。
(二)室间质量评价
开展流式细胞临床检测的实验室应制订室间质量评价程序,定期参加室间质评或能力验证计划。质评标本的检测流程应与临床标本的检测流程保持一致,以确保检测结果的可比性和真实性。应及时反馈室间质量评价结果,总结经验并改进检测方法,具体要求包括反馈分析、根本原因分析、纠正措施、预防措施以及所有质量保证活动和改进措施的记录。
我国于2024年4月2日发布了中华人民共和国卫生行业标准WS/T 360-2024流式细胞术检测外周血淋巴细胞亚群指南(代替WST 360—2011)。

![]() WST 360-2024 流式细胞术检测外周血淋巴细胞亚群指南.pdf
WST 360-2024 流式细胞术检测外周血淋巴细胞亚群指南.pdf
7.2.3 室内质控 (Internal quality control,IQC)
应首选商品化全血质控品进行室内质控。质控品应和患者样品同时进行免疫荧光染色,并在患者标本检测前进行上机测定和数据分析。如暂时无法获取商品化质控品,可采用接近医学决定水平(如HIV+患者CD4+淋巴细胞计数低至200个/μL)的复查样品(建议选取采样后24小时内的样品)进行质控。
检测当日至少做一次质控,并至少包括两个浓度水平,CD4+T细胞的绝对细胞计数应包括低值浓度水平质控,并做好相应质控记录。实验室应建立每一批次质控品的靶值和可接受范围,不可直接引用说明书提供的质控范围。更换新批号质控品前,可通过每日检测4次质控品(不同时间点),连续5天收集20次数据,计算均值。均值作为新批次靶值,结合既往累计CV值推算SD。应至少选择13S和22S作为失控判断标准,应有相应的失控纠正措施。使用全血质控品时,应按照说明书操作。
菁良临床质控一站式解决方案
菁良通过自主研发和国产化生产,向体外检测行业用户及合作伙伴提供全球领先的临床实验室质量控制解决方案,协助医学实验室实现全面质量管理。现已推出专业的质控管理软件及ISO15189质量管理体系咨询服务,第三方质控品涵盖免疫诊断、生化诊断、分子诊断等体外诊断细分领域。
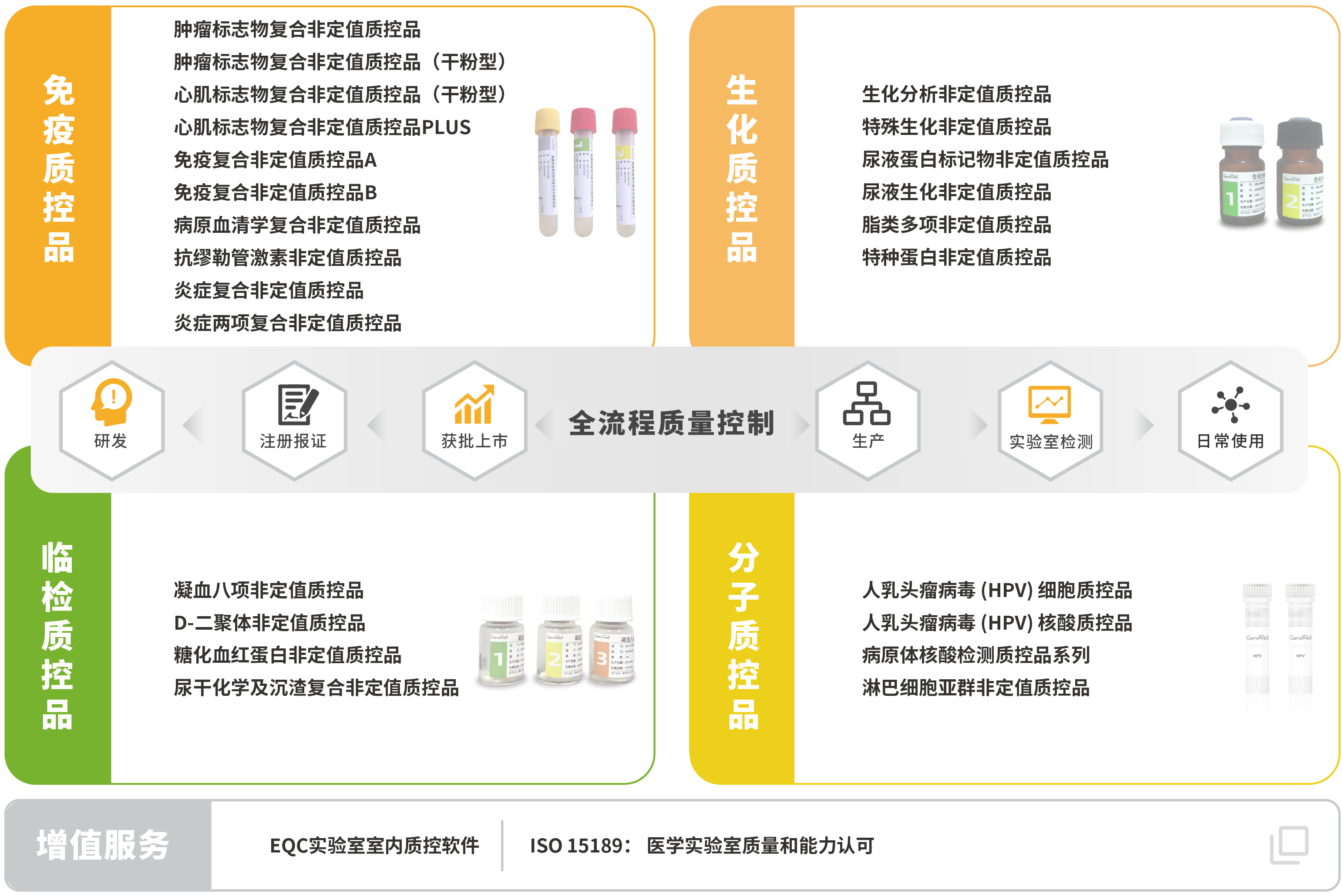
关于菁良
菁良科技(深圳)有限公司是全球领先的提供体外诊断标准品与质控品的研发创新型高科技企业。
菁良通过自主研发的平台,向体外检测行业用户及合作伙伴提供全球领先的标准物质、第三方质控产品和企业参考品服务,助力提高行业检测准确率。参与多项由检测领域行业龙头和监管机构发起的标准制定工作,多次支持由临检中心发起的室间质量评价 (EQA)/能力验证项目。
菁良秉承着“精准制标,匠心良造”的理念,怀抱着“提高体外检测准确率,助力精准医学快速发展”的愿景,致力于建立规范化的中国体外检测金标准平台。
